
【互傳媒/記者 林明佑/台中 報導】中國醫藥大學附設醫院院長周德陽研究團隊攜手聖安生醫,共同開發創新奈米三特異性T細胞銜接抗體「Nb-TriTE」抗癌藥物 (SOA101),成功完成臨床前研究,針對肺癌、乳癌等多種實體癌症,為癌症治療帶來重大突破,並將研究成果發表於國際知名期刊《Advanced Science》並獲得高分肯定,近期將提出美國FDA人體臨床試驗申請,為癌症患者提供全新治療選擇,解決全球癌症治療長期以來的瓶頸問題。
 ▲周德陽院長指出,目前市面上的抗體藥物大多受限於單一靶點,SOA101作為新一代奈米三特異性抗體,能夠同時標靶腫瘤表面的PD-L1與HLA-G,解決腫瘤細胞對單一免疫檢查點抗體產生抗性的問題。(中醫大附醫提供)
▲周德陽院長指出,目前市面上的抗體藥物大多受限於單一靶點,SOA101作為新一代奈米三特異性抗體,能夠同時標靶腫瘤表面的PD-L1與HLA-G,解決腫瘤細胞對單一免疫檢查點抗體產生抗性的問題。(中醫大附醫提供)做為全球第一個奈米三特異性抗體抗癌藥物,SOA101主要特色是設計兩個奈米抗體標靶癌細胞上兩個免疫檢查點,對抗癌細胞逃避身體免疫偵測,降低癌細胞抗藥性,提升藥物抗癌療效。在肺癌腫瘤動物模式實驗中,SOA101展現出顯著的療效,且未見不良反應,在多種實體腫瘤中均展現療效,包括乳癌、大腸癌、口腔癌及卵巢癌,顯示其具備搶攻免疫檢查點藥物市場的潛力。
 ▲聖安生醫總經理江宏哲表示,SOA101有兩個全球第一,全球第一個奈米三特異性抗體,與全球第一個雙免疫檢查點抑制抗體。聖安為全球前十大三特異性抗體新藥開發廠商之一,未來新藥上市將在全球抗癌藥物市場中佔據領先地位。(中醫大附醫提供)
▲聖安生醫總經理江宏哲表示,SOA101有兩個全球第一,全球第一個奈米三特異性抗體,與全球第一個雙免疫檢查點抑制抗體。聖安為全球前十大三特異性抗體新藥開發廠商之一,未來新藥上市將在全球抗癌藥物市場中佔據領先地位。(中醫大附醫提供)周德陽院長指出,免疫治療及藥物開發日新月異,目前市面上的抗體藥物大多受限於單一靶點,長期使用可能導致腫瘤細胞產生新的免疫檢查點蛋白,進而對原有的抗體藥物產生抗藥性。SOA101作為新一代奈米三特異性抗體,能夠同時標靶腫瘤表面的PD-L1與HLA-G,解決腫瘤細胞對單一免疫檢查點抗體產生抗性的問題。
 ▲聖安生醫處長邱紹智指出,目前已完成與美國食品和藥物管理局(FDA)的pre-IND會議,並獲得正向回應,並已向FDA提交Phase I/IIa臨床試驗申請,若獲批准,SOA101將成為全球首個進行“First-in-Human”臨床試驗的三特異性“奈米”抗體藥物。(中醫大附醫提供)
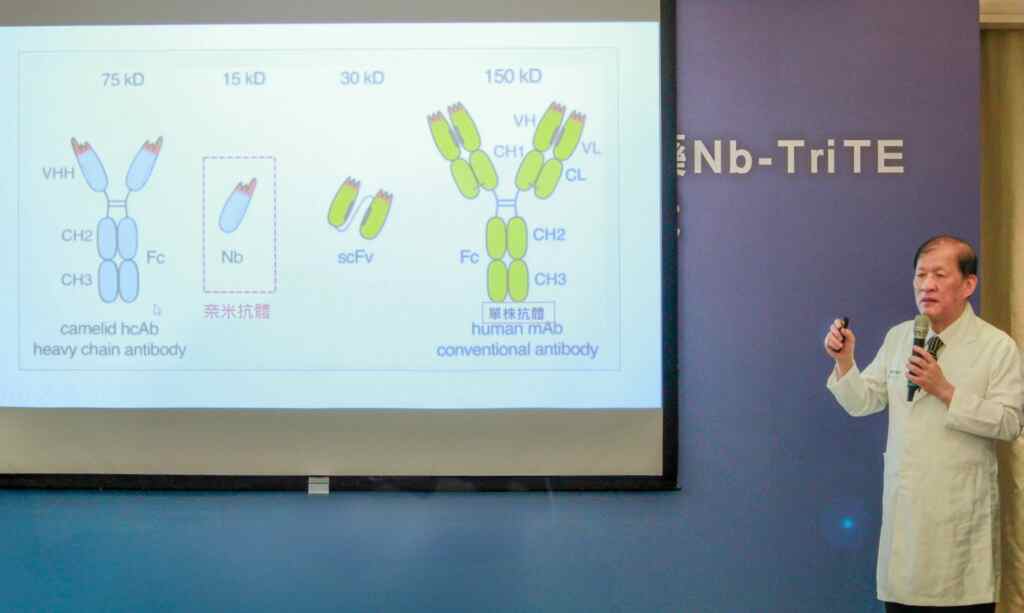
▲聖安生醫處長邱紹智指出,目前已完成與美國食品和藥物管理局(FDA)的pre-IND會議,並獲得正向回應,並已向FDA提交Phase I/IIa臨床試驗申請,若獲批准,SOA101將成為全球首個進行“First-in-Human”臨床試驗的三特異性“奈米”抗體藥物。(中醫大附醫提供)周德陽院長進一步解釋,奈米抗體屬於第三代抗體技術,優勢在其分子量僅為單株抗體的十分之一,能更好地穿透腫瘤微環境,耐受溫度變化,並且抗體之間的互相干擾較低,這是SOA101利用“奈米級”抗體所突破的結構設計難點,使SOA101成為癌症治療中的潛在變革者,為數百萬癌症患者帶來新的希望。」
聖安生醫總經理江宏哲表示,SOA101有兩個全球第一,全球第一個奈米三特異性抗體,與全球第一個雙免疫檢查點抑制抗體。根據科睿唯安的資料顯示,聖安為全球前十大三特異性抗體新藥開發廠商之一,未來新藥上市將在全球抗癌藥物市場中佔據領先地位。」
為了加速SOA101的臨床應用,聖安生醫已完成與美國食品和藥物管理局(FDA)的pre-IND會議,並獲得正向回應。該公司已能量產GMP等級的藥物,並完成相關申請文件準備,已向FDA提交Phase I/IIa臨床試驗申請,若獲批准,SOA101將成為全球首個進行“First-in-Human”臨床試驗的三特異性“奈米”抗體藥物。
聖安生醫的研發團隊也在推動另一個技術平台「標靶外泌體藥物遞送平台」(SOB100) 的系列藥物研發,榮獲知名藥廠默克(Merck)設立的新興生物科技獎助計畫(Advance Biotech Grant Program)第11屆默克(Merck)特別獎。該平台首個產品 HLA-G靶向性外泌體預計將於今年底向FDA提交Phase I臨床試驗申請。
